本帖最后由 Johnny 于 2020-5-20 16:41 编辑
Codiak公布新的临床前数据——engEx™工程外泌体驱动新型分子药物的潜力- exoVACC™模块化疫苗平台可诱导强大的全身和组织驻留T细胞反应
- 工程化的外泌体可靶向多种细胞类型
近日,将工程化外泌体作为一种新型生物药物进行开发的领先企业Codiak BioSciences公司,公布其专有的engEx平台的最新临床前数据。重点包括,新的临床前数据证明,与标准疫苗方法相比,其exoVACC疫苗平台可驱动强大的适应性免疫反应,以及有关利用engEx指导体外和体内多种细胞趋向性的能力的首批数据。这些数据在美国基因与细胞治疗学会(ASGCT)第23届年会上公布,证明了工程改造的外泌体具有广阔的潜力,可作为新型分子药物解决复杂的免疫相关疾病的基础。
外泌体是重要的细胞间通讯系统,有助于分子有效载荷在细胞之间的转移。它们由外泌体表面上复杂的蛋白质和糖蛋白网络介导,这些网络在细胞的趋向性、摄取和免疫细胞信号传导中起作用。利用其engEx平台,Codiak可以对具有不同特性的外泌体进行工程改造,为它们加载各种类型的治疗分子并改变向性,从而使它们达到特定的细胞靶标。Codiak正在开发候选外泌体产品,以靶向全身多种途径来治疗各种癌症,并通过其exoVACC模块化疫苗平台来增强针对多种抗原的免疫反应。
Codiak BioSciences总裁兼首席执行官道格拉斯·威廉姆斯(Douglas E. Williams)表示:“我们在engEx平台上产生的结果继续证实,我们的engEx工程外泌体有潜力成为一种全新的方式,能够解决未满足需求的疾病。令人兴奋的是,在这里,我们首次展示了从exoVACC平台产生的数据,与传统疫苗制剂相比,我们可以通过多种给药途径刺激免疫反应。我们的exoVACC数据表明在癌症和传染病中具有广泛的潜在应用。” exoVACC诱导强效的全身和组织驻留免疫反应 exoVACC利用Codiak设计的外泌体的独特特性,将抗原和佐剂同时选择性地递送至抗原呈递细胞(APC),从而驱动针对抗原的整合的先天、细胞和抗体介导的免疫反应。该平台的模块性允许在单个外泌体内掺入多种复合抗原、佐剂、靶向配体和免疫共刺激分子,以调整适当的免疫应答。
为了评估通过不同给药途径的免疫反应,外泌体被改造为使用专有支架蛋白BASP-1在腔中表达卵清蛋白模型抗原(OVA),并装有STING激动剂佐剂。与常用的可溶性OVA抗原和AddaVax®佐剂皮下注射(SC)相比,单剂量exoVACC皮下注射(SC)、鼻内注射(IN)或静脉注射(IV)时,诱导的脾脏抗原特异性CD8+ T效应记忆细胞数量增加约9至20倍。为了评估CD8+ T细胞反应的影响,在淋巴瘤肿瘤模型中评估了exoVACC。与对照相比,exoVACC减弱或完全抑制了EG7 OVA的肿瘤生长,并延长了生存期。
此外,IN施用exoVACC导致在肺中产生组织驻留CD8+ T细胞,而常用的佐剂,如Heltinol®,与可溶性OVA或与外泌体相关的OVA共同施用时不会在肺中产生组织驻留CD8+ T细胞。这些记忆组织驻留T细胞提供了针对呼吸道病毒(如SARS-CoV-2)的第一道防线。
公司Nikki Ross博士于2020年5月12日发表了题为“Induction of Potent Systemic and Tissue Resident Immune Responses by exoVACC™: a Novel Exosome-Based Vaccine Platform”的口头报告。
工程外泌体可具有特定的细胞倾向性,实现目标有效载荷靶向输送 体外和体内多项研究的结果表明engEx平台具有重定向外泌体向性并驱动各种独特细胞类型摄取的能力。外泌体表面显示了几种类型的靶向结构域。在体内,实现了对树突状细胞和T细胞的向性增加。具体而言,用靶向结构域修饰外泌体会导致摄入外泌体的靶细胞数量增加,摄入anti-Clec9A外泌体的树突状细胞增加4倍,而摄取anti-CD3外泌体的T细胞高4.7倍;与不具靶向性的对照外泌体相比,每个细胞摄取的外泌体数量也更多,anti-Clec9A外泌体高6倍,anti-CD3的外泌体高13倍。
向性改变导致药理学有效载荷传递增加,负载有STING激动剂的anti-Clec9A外泌体在原代小鼠树突状细胞中诱导的促炎细胞因子水平高达无靶向对照的15倍。此外,初步的体内数据表明,与无靶向的对照相比,这些anti-Clec9A外泌体将所需的STING激动剂剂量降低了10倍,以控制肿瘤的生长并诱导针对肿瘤相关抗原的免疫反应。
公司Monique Kauke博士于2020年5月15日发表了题为“Engineering Exosomes with Altered Cellular Tropism for Targeted Payload Delivery In Vivo”的口头报告。
关于engEx™平台
engEx平台是Codiak专有的外泌体治疗“引擎”,用于设计和制造新颖的外泌体候选产品,旨在针对全身的多种途径。使用该平台,Codiak可以设计出具有精确设计特性的外泌体,并整合各种类型的生物活性分子并将其引导至特定的细胞类型和组织。这些外泌体通过细胞摄取、膜与膜的相互作用或两者的结合而参与,并被设计成改变受体细胞生物学功能以产生预期的治疗效果。Codiak正在建立广泛的engEx产品候选产品管线,这些产品可能对许多疾病的治疗产生变革性影响。
Codiak最新研发管线
候选产品exoSTING™的实验数据:
候选产品exoIL-12™的实验数据: 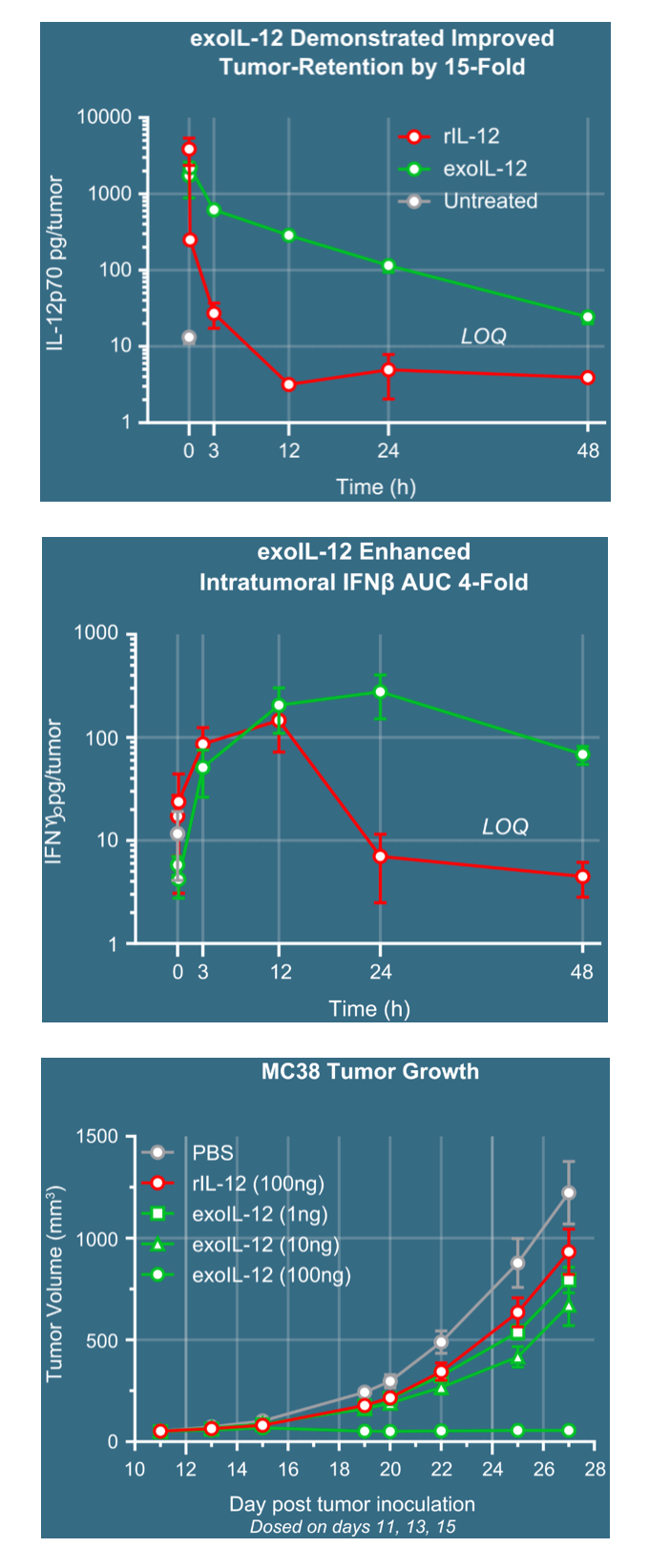 参考资料:Codiak公司官网
|  /1
/1 
 |Archiver|手机版|外泌体之家 | exosomes & microvesicles
|Archiver|手机版|外泌体之家 | exosomes & microvesicles
